Simulador de concentración química y solubilidad
🧪 Laboratorio online de Disoluciones
Entender la concentración es clave en química. Con este laboratorio virtual, podrás calcular la Molaridad, ver cómo la temperatura afecta a la solubilidad y analizar los resultados con gráficas interactivas.
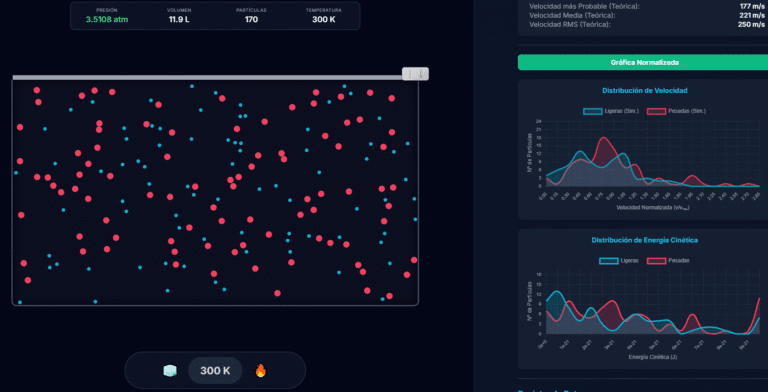
Si quieres mas, isita nuestro nuevo y espectacular simulador de cinética molecular
- 🔗 Categoría: Química | Disoluciones ↗️
- 🎓 Nivel educativo: Bachillerato
- ⚙️ Dificultad: Media (4/10)
- 📈 Visitas: 94
📎 Código para incrustar
¿Eres profe, divulgador o webmaster?
Puedes incrustar esta simulación en tu web o blog sin problema.
Solo pedimos dos cosas básicas:
- ✅ Que cites la fuente: AulaQuest.com
- 🚫 Que no la uses con fines comerciales
Este es el código que puedes copiar:
<iframe
src="https://aulaquest.github.io/simulador-de-concentracion-quimica/"
width="100%"
height="560"
style="border: 1px solid #ccc; border-radius: 8px;"
allowfullscreen
title="Simulación 2ª Ley de Kepler"></iframe>Exploración Interactiva de las Disoluciones Químicas
¿Cuál es el objetivo de este laboratorio interactivo de disoluciones y cómo se usa?
Este laboratorio interactivo de disoluciones es una potente herramienta para visualizar y manipular conceptos clave de química. Es un completo simulador de concentración química que te ayuda a entender la relación entre concentración y solubilidad.
Controles Principales:
- Añadir Agua: Aumenta el volumen (V) del disolvente.
- Añadir Soluto: Arrastra el salero para añadir moles (n) de soluto.
- Drenar: Elimina parte de la disolución completa (agua + soluto).
- Evaporar: Elimina solo el agua (disolvente). La concentración aumenta.
- Temperatura: Mantén pulsado +/- para calentar o enfriar la disolución.
¿Cómo se usa este simulador de concentración química para calcular la Molaridad?
La Molaridad (M) es la medida de concentración más visible en este laboratorio interactivo. Se define como los moles de soluto por el volumen total de la disolución en litros.
Molaridad (mol/L) = Moles Soluto / Volumen Disolución (L)
1. Prepara cualquier disolución, por ejemplo, 0.8 L de agua y añade algo de Azúcar.
2. Anota los valores de "Moles en Disolución" y "Volumen" que muestra el panel principal.
3. Aplica la fórmula y comprueba que tu resultado es idéntico al valor de "Concentración" que te da el simulador.
¿Cómo se calcula la Molalidad (m) en este laboratorio interactivo?
La Molalidad (m) se define como los moles de soluto por kilogramo de disolvente. A diferencia de la Molaridad, no cambia con la temperatura, una propiedad clave en el estudio de la solubilidad.
Molalidad (mol/kg) = Moles Soluto / Masa Disolvente (kg)
1. Ve al panel "Datos para Cálculos".
2. Anota los "Moles en Disolución" y la "Masa Disolvente (kg)".
3. Simplemente divide el primer valor entre el segundo para obtener la molalidad de tu disolución.
¿Cómo determinar el Porcentaje en Masa con el simulador?
El Porcentaje en Masa indica cuántos gramos de soluto hay en 100 gramos de disolución total. Es otra forma fundamental de expresar la concentración.
% Masa = (Masa Soluto (g) / Masa Disolución (g)) * 100
En "Datos para Cálculos", localiza la "Masa Soluto (g)" y la "Masa Disolución (g)". Divide la masa del soluto entre la masa total y multiplica el resultado por 100.
¿Cómo calcular la Fracción Molar (X) en una disolución?
La Fracción Molar (X) es la relación entre los moles de un componente y los moles totales de la disolución. Es una medida de concentración adimensional.
X_soluto = n_soluto / (n_soluto + n_agua)
Para ello, primero necesitas los moles de agua (H₂O), que puedes obtener a partir de su masa y su masa molar (~18.015 g/mol).
1. Anota los "Moles en Disolución" (n_soluto) y la "Masa Disolvente (kg)".
2. Calcula los moles de agua: n_agua = (Masa Disolvente (kg) * 1000) / 18.015.
3. Aplica la fórmula de la fracción molar para encontrar X del soluto.
¿Cuándo y cómo se calculan las Partes por Millón (ppm)?
Las ppm se usan para expresar concentraciones muy pequeñas. Representan los miligramos de soluto por cada kilogramo de disolución.
ppm = (Masa Soluto (mg) / Masa Disolución (kg))
1. Toma la "Masa Soluto (g)" y multiplícala por 1000 para obtenerla en miligramos (mg).
2. Toma la "Masa Disolución (g)" y divídela por 1000 para obtenerla en kilogramos (kg).
3. Divide el resultado del paso 1 entre el del paso 2 para obtener las ppm.
¿Cómo se relaciona la Concentración y Solubilidad con la temperatura?
La solubilidad es el límite máximo de concentración que se puede alcanzar a una temperatura dada. Este límite se llama Concentración de Saturación (Csat).
- Insaturada: Cuando la concentración actual (C) es menor que la Csat.
- Saturada: Cuando C = Csat. Se ha alcanzado el límite.
- Con Precipitado: Hay más soluto del que se puede disolver; la concentración del líquido es igual a Csat.
Pregunta Clave: ¿Aumenta la concentración al calentar?
Depende. Si la disolución está INSATURADA, NO. Si está SATURADA CON PRECIPITADO, SÍ, porque el calor aumenta la solubilidad (Csat) y permite que más sólido se disuelva.
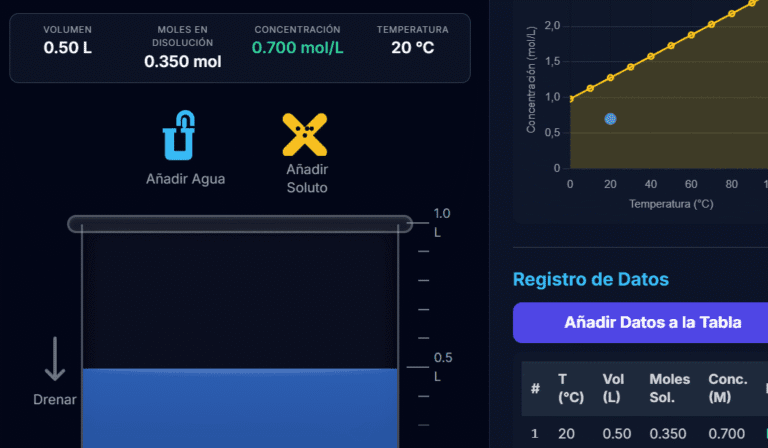
¿Cómo interpreto la Gráfica de Concentración vs. Temperatura?
Esta gráfica es una herramienta visual clave en nuestro laboratorio interactivo de disoluciones.
- Línea Amarilla: Muestra el límite de solubilidad (Csat). Representa la máxima concentración posible a cada temperatura.
- Punto Azul: Muestra el estado actual de tu disolución.
Observar la posición del punto azul respecto a la línea te permite saber al instante si tu disolución es insaturada o saturada.
Añade Cloruro de Níquel (II) hasta que haya precipitado. Ahora calienta la disolución y observa cómo el punto azul "persigue" a la línea amarilla hacia arriba mientras el sólido se disuelve.
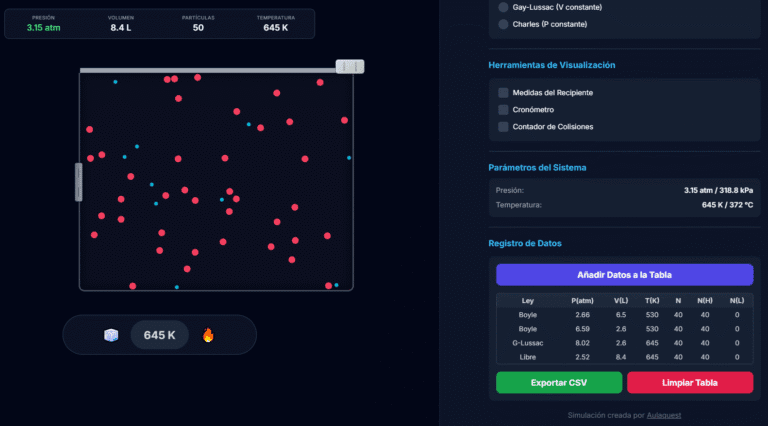
¿Cómo registrar datos para un informe de laboratorio?
Para cualquier informe sobre concentración y solubilidad, es útil registrar tus datos experimentales.
- Añadir Datos a la Tabla: Guarda una "foto" del estado actual de la disolución.
- Exportar CSV: Descarga la tabla en un archivo
.csv, compatible con Excel o Google Sheets, para analizar tus resultados.
Realiza un experimento registrando datos a distintas temperaturas. Exporta el CSV y crea tu propia gráfica de solubilidad.
Zona de Actividades de tu Profesor
Introduce la clave de acceso que te ha proporcionado tu profesor para cargar la actividad y comenzar a trabajar.
¿Tu última clase con la simulación fue un éxito?
Si has usado una de nuestras simulaciones para crear una actividad que funcionó de maravilla, te invitamos a compartirla. Crear una actividad es muy fácil y tu experiencia puede ser la inspiración que otro docente necesita.
- 💡 Transforma tu experiencia en un recurso valioso para miles de profes.
- 🔥 Ayuda a otros a encender la misma pasión que tú lograste en tu aula.
- 🌍 Forma parte de una comunidad que cree en compartir para crecer juntos.
*Esto es solo para profes. Si lo eres, pide tu acceso.
Simulaciones en Química
No necesitas dar la clase perfecta
Solo necesitas que tus alumnos entiendan. Usa nuestras simulaciones y cambia el chip sin perder tiempo ni energía.
Zona Profe